盐 (化学)
此條目需要补充更多来源。 (2021年8月9日) |

盐在化学中,是指一类金属离子或銨根離子(NH4+)与酸根离子或非金屬離子结合的化合物,如硫酸钙,氯化铜,醋酸钠,一般来说盐是複分解反应的生成物,如硫酸与氢氧化钠生成硫酸钠和水,也有其他的反应可生成盐,例如置换反应。
盐分为單盐和合盐,單盐分為正盐、酸式盐、碱式盐,合盐分為複盐和錯盐。其中酸式盐除含有金属离子与酸根离子外还含有氢离子,碱式盐除含有金属离子与酸根离子外还含有氢氧根离子,複盐溶於水時,可生成與原盐相同离子的合盐;錯盐溶於水時,可生成與原盐不相同的複雜离子的合盐——配合物。
通常在標準狀況下,不可溶的盐會是固態,但也有例外,例如熔盐及离子液体。可溶盐的溶液及熔盐有导电性,因此可作為電解質。包括細胞的細胞質、血液、尿液及礦泉水中都含有許多不同的盐類。
强碱弱酸盐是强碱和弱酸反应的盐,溶于水显碱性,如碳酸钠。而强酸弱碱盐是强酸和弱碱反应的盐,溶于水显酸性,如氯化铁。
盐的性质
[编辑]在化學上,鹽是由陽離子(正電荷離子)與陰離子(負電荷離子)所組成之電中性(不帶電荷)離子化合物。
- 碱(可溶)+盐(可溶)→新碱+新盐
- 和盐发生反应。复分解反应。
- 盐(可溶)+盐(可溶)→两种新盐
- 和某些金属反应。置换反应
- 盐+金属(某些)→新金属+新盐 反应中的金属一定要比盐中的金属活泼才可以把它给置换出来。请看金属活动性。
盐的分类
[编辑]单盐
[编辑]- 正盐:
正盐是鹽类的一种,既不含能电离的氢离子,又不含氢氧根离子。 正盐是酸和碱完全中和的产物[1],但正盐的水溶液不一定显中性,如(碳酸钠)溶液显碱性,(硫酸铵)溶液显酸性。酸跟碱完全中和生成的盐中,不会有酸中的氢离子,也不会有碱中的氢氧根离子,只有金属阳离子和酸根离子,这样的盐为正盐。
- 酸式盐:

酸式盐是盐类的一种,由阳离子和多元酸的不完全电离酸根阴离子组成。由于阴离子中含有在水中可电离的氢原子,因此被称作“酸式”盐[1]。但实际上,只有强酸(如硫酸)及少部分中强酸(如磷酸)的酸式盐呈酸性,大多数弱酸的酸式盐都因阴离子的水解而显碱性。
要注意的是,酸式盐在以离子晶体形式存在时,阴离子并不电离出氢离子,氢离子是酸式酸根离子的一部分。在熔融状态下,酸根离子也不电离。
- 碱式盐:
碱式盐是盐类的一种,除了含有金属离子和酸根离子外,还含有氢氧根或氧離子的盐类;也可认为是碱的氢氧根没有被酸完全中和所得的产物。 含羥基的鹼式盐又稱為羥基盐,可視為金屬離子、氫氧根及阴離子合成的鹽類,如碱式碳酸銅()、碱式氯化镁()等為羥基盐。
含氧基的鹼式盐稱為氧化鹽,可視為金屬離子、氧離子(O2-)及阴離子合成的鹽類。如鹼式碳酸鉍()即為氧化盐。
合盐
[编辑]- 複盐:
复盐是指含有两种或以上的同种晶型的简单盐类[1],属于化合物,溶于水会离解出所有的离子。复盐通常可由混合这两种盐饱和溶液并结晶而制得。在自然界中廣泛存在,如明礬就是天然而有廣泛應用的複鹽。
络盐
[编辑]- 錯盐:
錯盐有配位单元的化合物。
盐的属性
[编辑]颜色
[编辑]盐的颜色可以是纯淨透明的(如氯化钠)、不透明的或者是带有金属光泽的(如黄铁矿)。大多数情况下盐表面的透明或不透明只和构成该盐的单晶体有关。当光线照射到盐上时,就会被晶界(晶体之间的边界)反射回来,大的晶体就会呈现出透明状,多晶体聚集在一起则会看起来更像白色粉末一样。
盐有许多颜色,例如(溶液):
大部分矿物质、无机色素以及很多人工合成的有机染料都是盐,有一些盐能够呈现出其它颜色是过渡元素的d轨道存在未成对电子导致的。
味道
[编辑]不同的盐可以激发不同的味觉,例如咸味(氯化钠)、甜味(乙酸铅[2],若大量食用会导致铅中毒)、酸味(酒石酸氢钾)、苦味(硫酸镁)或鲜味(谷氨酸钠)[3]。
气味
[编辑]强酸或强碱盐(强盐)是不可挥发的,且没有气味。而弱酸或弱碱盐(弱盐)则会根据共轭酸碱对而产生不同的气味(例如醋酸盐则会有醋酸的味道,氰化氢则会有苦杏仁味等),此外弱酸或弱碱盐还会挥发和分解,并且由于水解反应和弱盐合成的反应是可逆反应,因此当有水分存在时会加速弱盐的分解。
溶解度
[编辑]許多離子化合物都可以溶解在水或是類似的溶劑中,化合物的溶解度和組成的陰離子和陽離子以及溶劑都有關,因此有一特定的關係。陽離子當中,所有鈉離子、鉀離子及銨離子的鹽均可溶於水;而陰離子中,硝酸鹽離子及碳酸氫鹽離子的鹽類可在水中溶解。除了硫酸鋇、硫酸鈣及硫酸鉛外,大部份的硫酸鹽離子的鹽類也都可以溶於水。而鹵素鹽(氯、溴、碘),則汞、銅、銀、鉈、鉛不溶。不過若離子之間的鍵結很強,產生高度穩定的固體,在水中也就不易溶解,例如大部份的碳酸鹽就不溶於水,例如碳酸鉛及碳酸鋇等。 盐的溶解性口诀:
钾钠铵盐都易溶,
硝酸盐遇水无影踪,
硫酸盐不溶铅和钡,
盐酸盐不溶银亚汞,
碳酸盐除钾钠铵外都不溶。
系统命名法
[编辑]一般而言,无氧酸盐的名字是非金属元素名称在前,金属元素名称在后,两者名字之间添加“化”,称为“某化某”。如果是含氧酸盐,则盐的名称为酸的名称后面之间添加元素名称,称为“某酸某”。如果某种金属元素有多个化合价,那么低化合价形成的盐的名称是在金属元素名称前添加“亚”,例如铜元素的氯化物中,如果铜的化合价为+2价,那么形成的盐CuCl2称为“氯化铜”,如果化合价为+1价,形成的盐CuCl称为“氯化亚铜”。
含有相同阳离子或阴离子的一类盐一般都会统称为“某盐”,例如“钠盐”、“硫酸盐”等。
常见的形成盐类的阳离子包括:
常见的形成盐类的阴离子包括:
- 乙酸根CH3COO−(乙酸)
- 碳酸根CO32−(碳酸)
- 氯離子Cl−(盐酸)
- 氰化物C≡N−(氰化氢)
- 硝酸根NO3−(硝酸)
- 亚硝酸根NO2−(亚硝酸)
- 磷酸根PO43−(磷酸)
- 硫酸根SO42−(硫酸)
- 硼酸根BO33- (硼酸)
有機離子的鹽類
[编辑]一般鹽類會歸類為無機化合物,但也有一些有機化合物的鹽類,例如有機酸的鹽類就是有機化合物。其中較重要的是羧酸鹽,例如乙酸根CH3COO−和鈉離子Na+會形成乙酸鈉,和銅離子Cu2+會形成乙酸銅。乙酸只有一個COOH基,只帶-1價,柠檬酸有三個COOH基,帶-3價,形成的鹽類有柠檬酸鈉和柠檬酸鈣根,乙酸鹽和柠檬酸鹽的陰離子和陽離子都以離子鍵鍵結,不像一般有機化合物以間用共價鍵鍵結,因此稱為鹽類。
這些鹽類中較常用的是羧酸鹽,其中也包括脂肪酸鹽。像肥皂就是由許多不同分子量脂肪酸鈉及脂肪酸鉀的混合物。這類長鏈脂肪酸的鹽類就沒有晶體的結構。
類似硫酸根SO42−的磺酸根也是有機酸根的一種,磺酸鹽是洗髮精及沐浴乳中常見的表面活性剂。醇類的酸性很弱,一般不會稱為酸,不過其羟基氢被金属取代后會形成醇盐。醇盐在水中會水解,產生對應的醇類,以下是醇盐和金屬鹼酐水解反應的比較。
| 水解反應 | |
|---|---|
| 乙醇鈉 | |
| 氧化鈉 | |

也有些有機的陽離子會形成鹽類,例如類似銨根離子(NH4+)的季铵阳离子,季铵阳离子是由一個氮原子和四個烷基()組成,帶一個正電荷。例如溴化十六烷基三甲铵中,十六烷基三甲铵離子是陽離子,和陰離子溴離子形成鹽類。實用的季铵鹽類也有類似的結構,季铵阳离子中只有一個長鏈的烷基,當溶於水中,陽離子有表面活性劑的作用。這類物質在生物體新陳代謝中有重要的作用,例如維生素B中的胆碱就是季铵鹽類。
在氨分子(NH3)中加入一個氫離子(H+)就變成銨離子(NH4+),同樣的在有機胺中加入一個氫離子就變成陽離子。例如一級胺(,R為烷基)加入一個氫離子就變成陽離子()這類的化合物比原來的化合物極性要強,因此在水中的溶解度比原來的化合物要高。例如一些含氮的藥物會和鹽酸反應來產生鹽酸胺類化合物,人體對於這類化合物的吸收度比原來的含氮藥物要好。也有些藥物是和溴化氫或氟化氫反應成類似的藥物。
內鹽也稱為兩性離子,是一種特殊的化合物,化合物中同時有帶正電及帶負電的原子,但是帶正電和負電的原子不同(在一些定義中限定是未具有相鄰正負電荷的化合物)[4],像許多胺基酸都屬於內鹽。若胺基酸中包含羧基()和一個胺基(),就是內鹽,會在不同的反應中呈酸性或是鹼性。不過內鹽和一般電解質不同,溶於水中只有微弱的導電性(兩性物質)。
有機陰離子和陽離子的例子
[编辑]| 有機化合物的陰離子 | ||
|---|---|---|
| 分類 | 舉例 | 結構 |
| 羧酸根 | 乙酸根 |  |
| 棕櫚酸根 |  | |
| 檸檬酸 |  | |
| 有機硫化物 | 十二烷基硫酸根 |  |
| 醇盐 | 乙醇盐 | |
| 有機化合物的陽離子 | ||
| 分類 | 舉例 | 結構 |
| 季銨陽離子 | 溴化十六烷基三甲銨 |  |
| 胆碱 |  | |
| 胺類 | 苯胺鹽類 |  |
| 有機化合物的內鹽 | ||
| 分類 | 舉例 | 結構 |
| 甜菜鹼 | 甜菜鹼 | 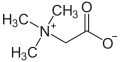 |
| 胺基酸 | 丙胺酸 | 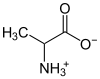 |
盐的製備
[编辑]盐可以通过化学反应而製備,包括有:
- 盐基与酸,例如NH3 + HCl → NH4Cl
- 金属与酸,例如Mg + H2SO4 → MgSO4 + H2
- 金属与非金属,例如Ca + Cl2 → CaCl2
- 碱与酸性氧化物,例如2 NaOH + Cl2O → 2 NaClO + H2O
- 酸与碱性氧化物,例如2 HNO3 + Na2O → 2 NaNO3 + H2O
- 盐也可以由不同的盐溶液混合,其中的离子发生重组,形成溶解度较低的盐(另见:溶解平衡),例如
參見
[编辑]参考资料
[编辑]- ^ 1.0 1.1 1.2 魏明通. 普通化學. 五南圖書出版股份有限公司. 2006: 24– [2014-06-12]. ISBN 978-957-11-4349-1. (原始内容存档于2014-07-28).
- ^ Nicholas Wade. 地球身世之謎. 知書房出版集團. 2004: p.159 [2014-06-12]. ISBN 9578320477. (原始内容存档于2014-07-14).
- ^ Y. Kawamura and M.R. Kare (编). 鮮味,基本味道. New York,NJ: Marcel Dekker. 1987.
- ^ 國際純化學和應用化學聯合會,化學術語概略,第二版。(金皮書)(1997)。在線校正版: (2006–) "zwitterionic compounds/zwitterions"。doi:10.1351/goldbook.Z06752



















