八羰基二鈷
| 八羰基二鈷 | |
|---|---|
| |

| |

| |
| IUPAC名 Octacarbonyldicobalt(Co—Co) | |
| 識別 | |
| CAS號 | 10210-68-1 |
| PubChem | 25049 |
| ChemSpider | 2007057 |
| SMILES |
|
| InChI |
|
| InChIKey | MQIKJSYMMJWAMP-UHFFFAOYAG |
| UN編號 | 3281 |
| EINECS | 233-514-0 |
| RTECS | GG0300000 |
| 性質 | |
| 化學式 | Co2(CO)8 |
| 摩爾質量 | 341.95 g·mol⁻¹ |
| 外觀 | 橙色晶體[1] |
| 密度 | 1.78 g/cm3[1] |
| 熔點 | 52 °C(325 K)(分解[1]) |
| 溶解性(水) | 不溶[1] |
| 蒸氣壓 | 0.7 mmHg (20 °C)[2] |
| 結構 | |
| 偶極矩 | 1.33 D(C2v異構體) 0 D(D3d異構體) |
| 危險性 | |
| MSDS | External SDS |
GHS危險性符號   
| |
| GHS提示詞 | Danger |
| H-術語 | H251, H302, H304, H315, H317, H330, H351, H361, H412 |
| P-術語 | P201, P260, P273, P280, P304+340+310, P403+233 |
| 主要危害 | 可能致癌 |
| NFPA 704 | |
| 閃點 | −23 °C(−9 °F)[2] |
| PEL | 無[2] |
| 致死量或濃度: | |
LD50(中位劑量)
|
15 mg/kg(大鼠,口服) |
| 相關物質 | |
| 相關金屬羰基配合物 | 五羰基鐵 九羰基二鐵 四羰基鎳 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
八羰基二鈷是一種無機化合物,化學式為Co2(CO)8。這種金屬羰基配合物是金屬有機化學和有機合成中的試劑及催化劑,也是有機鈷化學的中心[3][4]它被用於羰基合成,也就是將烯烴轉化成醛的催化劑。[5]
合成、結構與性質
[編輯]在氰化物存在條件下,通過鈷(II)鹽的高壓羰基化反應可製得八羰基二鈷。它是一種橙色易自燃的固體,對熱不穩定。它在溶液中存在兩種異構體[3][4],快速轉化:[6]
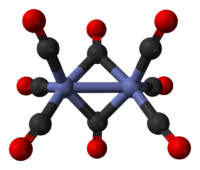
它的優勢異構體類似於Fe2(CO)9,只是少了一個橋連的羰基配體。Co-Co鍵的鍵長是2.52 Å,Co-CO端基和Co-CO橋連鍵長分別是1.80和1.90 Å。[7]這些異構體互變速度很快。占少數的這種異構體沒有橋連的CO配體,可以寫成(CO)4Co-Co(CO)4(D3d 對稱群)。優勢異構體中有兩個橋連的CO配體,特點是含有八面體配位的鈷,它可寫成(CO)3Co(μ-CO)2Co(CO)3(C2v 對稱群)。較少的這種異構體已經通過與C60共結晶製得。[8]
反應
[編輯]
還原
[編輯]八羰基二鈷可和鹼金屬和相關試劑(如鈉汞齊)反應,生成四羰基鈷酸鹽,後者和酸反應生成四羰基鈷酸:[4]
- Co
2(CO)
8 + 2 Na → 2 Na[Co(CO)
4] - Na[Co(CO)
4] + H+
→ H[Co(CO)
4] + Na+
和親電試劑的反應
[編輯]八羰基二鈷和鹵素反應,生成四羰基鹵化鈷:[9]
- Co
2(CO)
8 + Br
2 → 2 Br[Co(CO)
4]
- Co
2(CO)
8 + 2 NO → 2 Co(CO)
3NO + 2 CO
合成其它羰基配合物
[編輯]加熱八羰基二鈷將導致脫羰基反應,並形成四面體的原子簇化合物十二羰基四鈷:[4][11]
- 2 Co2(CO)8 → Co4(CO)12 + 4 CO
八羰基二鈷和其它金屬羰基配合物一樣,可以和鹵代烴反應。它和溴仿反應,生成甲爪基九羰基三鈷 HCCo
3(CO)
9:[12]
- 9 Co
2(CO)
8 + 4 CHBr
3 → 4 HCCo
3(CO)
9 + 36 CO + 6 CoBr
2
其它
[編輯]CO配體可以被三烴基膦配體取代,產生Co2(CO)8-x(PR3)x。這些體積龐大的衍生物是氫甲酰化反應選擇性更高的催化劑。「硬鹼」,例如吡啶,可使八羰基二鈷發生歧化反應:
- 6 C6H5N + 1.5 Co2(CO)8 → [Co(C6H5N)6][Co(CO)4]2 + 4 CO
Co2(CO)8也能催化葆森–侃德反應(Pauson–Khand reaction),也就是烯烴、炔烴與CO反應產生α,β-環戊烯酮衍生物的反應。
安全
[編輯]Co2(CO)8是一種揮發性的鈷(0)化合物,容易自燃。它受熱分解產生一氧化碳氣體。 [13]
參見
[編輯]參考資料
[編輯]- ^ 1.0 1.1 1.2 1.3 Record of Dicobaltoctacarbonyl in the GESTIS Substance Database from the IFA
- ^ 2.0 2.1 2.2 NIOSH Pocket Guide to Chemical Hazards. #0147. NIOSH.
- ^ 3.0 3.1 Pauson, Peter L.; Stambuli, James P.; Chou, Teh-Chang; Hong, Bor-Cherng. Octacarbonyldicobalt. Encyclopedia of Reagents for Organic Synthesis. John Wiley & Sons: 1–26. 2014. ISBN 9780470842898. doi:10.1002/047084289X.ro001.pub3.
- ^ 4.0 4.1 4.2 4.3 Donaldson, John Dallas; Beyersmann, Detmar. Cobalt and Cobalt Compounds. Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH. 2005. ISBN 3527306730. doi:10.1002/14356007.a07_281.pub2.
- ^ Elschenbroich, C.; Salzer, A. Organometallics: A Concise Introduction 2nd. Weinheim: Wiley-VCH. 1992. ISBN 3-527-28165-7.
- ^ Sweany, Ray L.; Brown, Theodore L. Infrared spectra of matrix-isolated dicobalt octacarbonyl. Evidence for the third isomer. Inorganic Chemistry. 1977, 16 (2): 415–421. doi:10.1021/ic50168a037.
- ^ Sumner, G. G.; Klug, H. P.; Alexander, L. E. The crystal structure of dicobalt octacarbonyl. Acta Crystallographica (International Union of Crystallography (IUCr)). 1964-06-01, 17 (6): 732–742. ISSN 0365-110X. doi:10.1107/s0365110x64001803.
- ^ Garcia, Thelma Y.; Fettinger, James C.; Olmstead, Marilyn M.; Balch, Alan L. Splendid symmetry: crystallization of an unbridged isomer of Co2(CO)8 in Co2(CO)8·C60. Chemical Communications (Royal Society of Chemistry (RSC)). 2009, (46): 7143. ISSN 1359-7345. doi:10.1039/b915083h.
- ^ Winzenburg, Mark Leo. Synthesis and reactivity of transition metal carbonylates. 1979. OCLC 6572244.
- ^ King, R. B. "Organometallic Synthesis, Volume 1: Transition-metal compounds" (1965) Academic Press. ISBN 0124080502
- ^ Chini, P. The closed metal carbonyl clusters. Inorganica Chimica Acta Reviews. 1968, 2: 31–51. doi:10.1016/0073-8085(68)80013-0.
- ^ Nestle, Mara O.; Hallgren, John E.; Seyferth, Dietmar; Dawson, Peter; Robinson, Brian H. μ3-Methylidyne and μ3-Benzylidyne-Tris(Tricarbonylcobalt). Inorganic Syntheses 20. 1980: 226–229. ISBN 9780470132517. doi:10.1002/9780470132517.ch53.
- ^ Cole Parmer MSDS. [2011-07-09]. (原始內容存檔於2011-09-27).


